J Lab Med 2004;28(6):525-533 c 2004 by Walter de Gruyter - Berlin - New York. DOI 10. 1 515/LabMed.2004.070
Validierung des MELISA-Tests zum Nachweis einer Metallüberempfindlichkeit1)
Validity of MELISA for metal sensitivity testing
Elizabeth Valentine-Thon1,* und Hans-Walter Schiwara2
1 MELISA (LTT) Center, Gemeinschaftspraxis für Laboratoriumsmedizin Dr. M. Sandkamp, B. Köster, Dr.R.Hiller, Bremen, Ge Deutschland
2 im Ruhestand, ehemals Labor Dr. Schiwara & Partner, Bremen, Ge Deutschland
Zusammenfassung
In dieser Studie wurden Reproduzierbarkeit, Sensitivität, Spezifität und Zuverlässigkeit des MELISA -Tests zum Nachweis von Metallüberempfindlichkeiten bei Patienten mit klinischen Symptomen einer Typ IV-Allergie gegen Metalle untersucht.
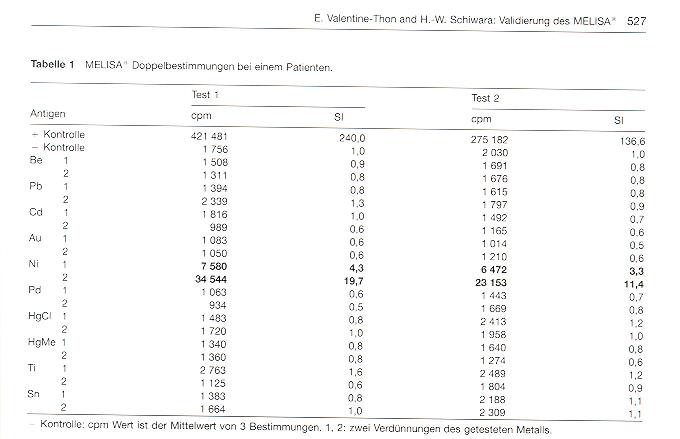
Von 250 Patienten wurde Blut im MELISA gegen bis zu 20 Metalle in 2 bis 3 verschiedenen Konzentrationen getestet. Häufigkeit und Verteilung positiver Testergebnisse, Sensitivität und Spezifität des Tests bei Patienten mit und ohne gesicherte oder vermutete Nickelallergie sowie die Bedeutung der Lymphozytenzahl und der Konzentration von anorganischem Quecksilber im Testsystem wurden untersucht. Darüberhinaus wurden für die Reproduzierbarkeitstestung 196 MELISA -Tests im Doppelansatz durchgeführt und die Intra- und Interassay-Variationen bei Patienten mit positivem Epikutan-Test für die entsprechenden Metalle bestimmt.
Von den 250 Patienten reagierten 26% gegen kein Metall, 36% gegen 1, 15% gegen 2, 12% gegen 3, 6% gegen 4 und 5% gegen >5 Metalle positiv im MELISA-Test. Die positiven Ergebnisse gegen die einzelnen Metalle wiesen folgende Häufigkeiten auf: Nickel (73%), Titan (42%), Cadmium (18%), Gold (17%), Palladium (13%), Blei (11%), Beryllium (9%), anorganisches Quecksilber (8%), Zinn (8%) und Phenylquecksilber (6%). Alle Patienten, bei denen eine Nickelallergie vermutet oder gesichert wurde (n = 15), reagierten im MELISA -Test positiv, während Patienten ohne Verdacht auf eine Nickelallergie entweder negativ (n = 6) oder sehr schwach positiv (n = 4) reagierten. Die Reaktivität des MELISA-Tests hängt von der Lymphozytenkonzentration ab: je höher die Lymphozytenkonzentration im Test, desto stärker die Reaktion. Eine Konzentration von > 0,5 m g/ml anorganischem Quecksilber verursacht bei den meisten Patienten eine nicht antigen-spezifische (mitogene) Reaktion. Die Reproduzierbarkeit betrug 94 % bei einem Stimulationsindex von > 3 und 99% bei einem Index von > 5 als Cut-off. Während die absoluten Intra- und Interassay-Stimulations-Indices variieren können, sind die quallitativen Ergebnisse in hohem Grade reproduzierbar.
Der MELISA-Test ist also reproduzierbar, sensitiv, spezifisch und zuverlässig für den Nachweis einer Metallunverträglichkeit bei gegen Metalle sensibilisierten Patienten.
Schlüsselwörter:Lymphozyten-Transformations-Test; MELISA'-Test; Metallunverträglichkeit; Nickel; Quecksilber.
R.Kiehl: Siehe dazu die Dateien (Buch-Kapitel) des RKI-Institutes unter www.rki-i.com, publikationen, materialien
Abstract
This study was carried out to evaluate the reproducibility, sensitivity, specificity, and reliability of the MELISA Test for detecting metal sensitivity in patients with clinical symptoms of a type IV hypersensitivity to metal.
Blood from 250 patients was tested in MELISA against up to 20 different metals in 2 to 3 concentrations. The frequency and distribution of metal reactivities, the sensitivity and specificity of nickel reactivity in patients with and without confirmed or suspected sensitivity to nickel, and the roles of lymphocyte concentration and concentration of inorganic mercury were analyzed. In addition, for reproducibility testing, 196 metal tests were performed in duplicate, and intra- and interassay variations of MELISA results were examined in patients patch-test positive for the relevant metal.
Among the 250 patients, reactivity to 0, 1, 2, 3, 4, or more than 5 metals was 26%, 36%, 15%, 12%, 6%, and 5%, respectively. Reactivity was most frequent to nickel (73%), followed by titanium (42%), cadmium (18%), gold (17%), palladium (13%), lead (11 %), beryllium (9%), inorganic mercury (8%), tin (8%), and phenylmercury (6%). All patients (n=15) with confirmed or suspected nickel allergy were positive in MELISA, while patients with no suspicion of nickel allergy were either negative (n = 6) or very low positive (n=4) in MELISA. MELISA reactivity is directly dependent on lymphocyte concentration: the higher the lymphocyte concentration per test, the stronger the reactivity. Concentrations of inorganic mercury > 0.5 m g/ml cause non antigen-specific (mitogenic) reactions in a majority of patients. The reproducibility rate was 94% using a cut-off of Stimulation Index > 3 or 99% using a cut-off of >5. While the absolute intra- and interassay Stimulation Index values may vary, the qualitative results are highly reproducible.
The MELISA Test is reproducible, sensitive, specific, and reliable for detecting metal sensitivity in metal-sensitive patients.
Keywords: lymphocyte transformation test; MELISA-Test; mercury; metal allergy; nickel.
Einleitung
Metallallergien werden konventionell im Epikutan-Test oder "Patch-Test" festgestellt, bei denen die vermutete allergisierende Substanz auf die Haut aufgebracht und nach 3-4 Tagen die Entwicklung von Erythemen, Papeln oder Bläschen an den Applikationsstellen geprüft wird. Eine positive Hautreaktion kann für eine spezifische Metallallergie sprechen, allerdings ist der Test nicht in der Lage, allergische von irritativen Reaktionen zu unterscheiden. Außerdem hat er eine geringe Sensitivität und eine schlechte Reproduzierbarkeit. Dazu scheint er nur für Allergene geeignet zu sein, für die die Haut das Zielorgan der Sensibilisierung ist. Ferner kann er selbst in vivo-Sensibilisierungen induzieren und bei bereits sensibilisierten Personen eine Exazerbation der Symptome verursachen [l -5]. Eine Alternative ist der Lymphozyten-Transformations-Test (LTT), bei dem Lymphozyten (Gedächtniszellen) des betreffenden Patienten zusammen mit dem zu untersuchenden Allergen 5-6 Tage kultiviert werden. Die dabei erfolgende Lymphoblastentransformation wird morphologisch nachgewiesen, die Messung der Lymphozytenproliferation erfolgt aufgrund des 3H-Thymidin-Einbaus. Der ursprünglich Mitte der sechziger Jahre für die Untersuchung der Histoinkompatibilität der HLA-Antigene der Klasse 11 entwickelte LTT [6, 7] wurde für die HLA Klasse 11-Antigentypisierung modifiziert [8] und auch vielfach zum Nachweis von Typ IV-Allergien gegen Medikamente, Metabolite, Krankheitserreger und Metalle verwendet [9-17]. Der LTT wurde ein Standard-Test zum Nachweis von Allergien gegen Nickel, Gold, Cobalt, Chrom und Palladium [l, 18-20]. Der LTT für Beryllium ist inzwischen der "Gold-Standard" für die Diagnose der Lungen-Berylliose [21, 22].
1994 veröffentlichten Stejskal et al. eine Modifikation des LTT zum Nachweis von Metallsensibilisierungen, den MELISA-Test (memory lymphocyte immunostimulation assay) [23]. Durch eine höhere Lymphozytenzahl im Test, die Wahl einer weder zytotoxischen noch mitogenen Metallkonzentration, die Depletion von Monozyten aus der Population der mononukleären Zellen und die Ergänzung der radiometrischen Ergebnisse durch eine morphologische Untersuchung konnten Sensitivität und Spezifität verbessert werden. In den letzten sechs Jahren wurden weltweit mehrere Laboratorien für die Durchführung des MELISA-Tests lizenziert und eine Reihe von wissenschaftlichen Arbeiten, die seine klinische Wertigkeit zeigen, veröffentlicht [24-26] oder befinden sich in Vorbereitung [27].
Das ehemalige Labor Dr. Schiwara & Partner in Bremen erhielt 1999 die Lizenz für die Durchführung des MELISA-Tests. Um die Kriterien für die Akkreditierung nach ISO 17025 zu erfüllen, wurde der Test hinsichtlich Sensitivität, Spezifität, Reproduzierbarkeit und
Zuverlässigkeit validiert. In der vorliegenden Studie werden die Ergebnisse dieser Validierung des MELISA -Tests zum Nachweis einer Metallsensibilisierung dargestellt.

1)Übersetzt nach dem Artikel: Valentine-Thon E and H-W Schiwara: Validity of MELISA for metal sensitivity testing. Neuroendocrinology Letters 2003;24:57-64 mit freundlicher Genehmigung von PG Fedor-Freybergh, Editor-in-Chief, Neuroendocrinology Letters *Korrespondenz: Dr. Elizabeth Valentine-Thon, MELISA (LTT) Center, Gemeinschaftspraxis für Laboratoriumsmedizin Dr. M. Sandkamp, B. Köster, Dr. R. Hiller, Norderoog 2, 28259 Bremen, Germany,Tel:0049-421-5725369,Fax:0049-421-571249,E-mail: evt@lanisa.de